Miranda J. Sadar, D.V.M., David McRuer, M.Sc., D.V.M., Dipl. A.C.V.P.M., Michelle G. Hawkins, V.M.D., Dipl. A.B.V.P. (Avian), and Aníbal G. Armién, D.V.M., M.Sc., Ph.D, Dipl. A.C.V.P.
Source: Journal of Zoo and Wildlife Medicine, 46(1):150-154.
Published By: American Association of Zoo Veterinarians
DOI: http://dx.doi.org/10.1638/2013-0247R4.1
URL: http://www.bioone.org/doi/full/10.1638/2013-0247R4.1
Перевод на русский язык: ветеринарный врач Лилия Калимулина, ветеринарный врач Валентин Козлитин
РЕЗЮМЕ: Самка взрослого дикого краснохвостого сарыча (Buteo jamaicensis) была доставлена в реабилитационный центр из-за неспособности стоять на лапах. При первичном обследовании выявлена двусторонняя гиперфлексия тазовых конечностей и гипертонус мышц разгибателей, нормальная болевая чувствительность кожи, положительный рефлекс отдергивания. Общеклинический анализ крови показал среднюю степень гетерофильного лейкоцитоза. Никаких аномалий не было замечено на рентгенографических снимках. После первоначального улучшения наступил регресс состояния и птица была эвтаназирована через 27 дней после поступления.
Вскрытие и гистологическое исследование выявило уменьшение диаметра позвоночного канала и ущемление спинного мозга в области 8-9 шейных позвонков со сливными гранулемами, содержащими кислотоустойчивые палочковидные бактерии в межтрабекулярном пространстве, в левом подключичном воздушном мешке и в краниальной части левого легкого.
Бактериологический посев и генетическое секвенирование материала из респираторных очагов выявили Mycobacterium avium avium. ПЦР в режиме реального времени фиксированных в парафине тканей спинного мозга дали положительный результат на M.avium комплекс.
При развитии у хищных птиц признаков неврологической вегетативной недостаточности в списке дифференциальных диагнозов следует рассматривать микобактериоз.
Дикая самка краснохвостого сарыча массой 1.34 кг поступила на обследование из-за невозможности стоять. При физикальном обследовании сарыч имел удовлетворительную упитанность (индекс упитанности 2.5/5) и билатеральный парез тазовых конечностей. На неврологическом осмотре у птицы обнаружена двусторонняя гиперфлексия тазовых конечностей и гипертонус мышц разгибателей, нормальная болевая чувствительность кожи, нормальный рефлекс отдергивания. Никаких гематом в области позвоночника не было обнаружено. Осмотр обоих крыльев и исследование функции черепно-мозговых нервов не выявил патологий. C правой стороны на уровне таза чуть сбоку от позвоночного столба была обнаружена покрытая струпом рана примерно 0,5 см в диаметре. Других ранений не обнаружили.
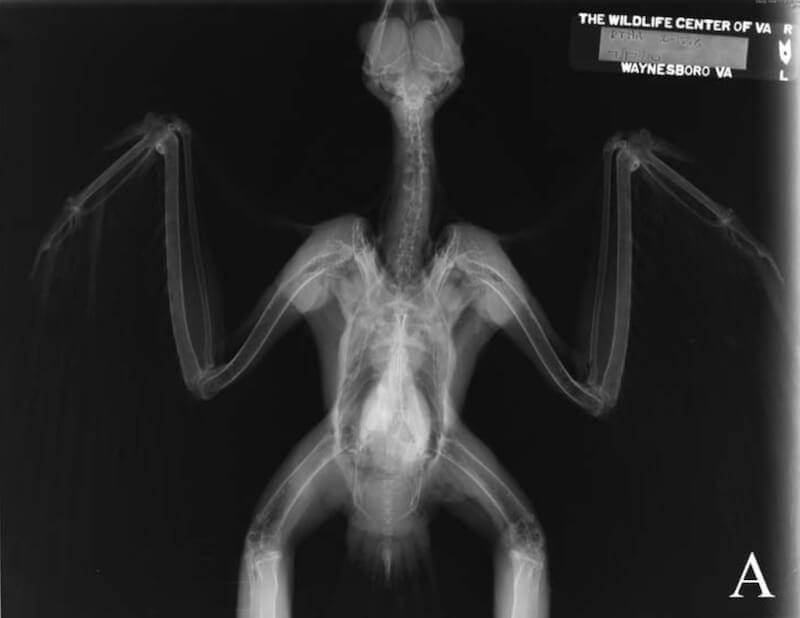
Результаты общего анализа крови (ОАК) выявили нормальный показатель гематокрита (37 % ; 37.2 +/- 4.6 % [mean 6 SD]) и умеренный лейкоцитоз (32.52 × 10 3/ мкл; 19.28 +/- 7.51 × 10 3 /мкл) с умеренной зрелой гетерофилией (23.41 × 10 3/ мкл; 10.81+/- 4.82 × 103 /мкл). Биохимический анализ сыворотки был ничем не примечательным. Были выполнены обзорные вентродорсальный и правая боковая рентгенограммы и никаких заметных отклонений не выявлено (Рис. 1). Центрифугирование помета не выявило паразитов. Плазма была исследованна на предмет выявления воздействия органофосфатов (холинэстераза 0,534 …) и цельная кровь была исследована на содержание свинца (˂0.034 мг) – все показатели были ничем непримечательны. ПЦР в реальном времени на Вирус Западного Нила из зева и клоаки была отрицательной.

Была начата поддерживающая терапия, включая: подкожное введение растворов (Раствор Рингера-лактат, Hospira, Lake Forest, Illinois 60045; 60 мл/кг в день); мелоксикам (Metacam, Boehringer Ingelheim Vet-medica, Inc., St. Joseph, Missouri 64506, USA; 0,4 мг/кг п/о 1 раз в день; амоксициллин/клавулановая кислота (Clavamox, Pfizer Animal Health, New York, New York 10017, USA; 125 mg/kg п/о 2 раза в день) и энрофлоксацин (Baytril, Bayer Corporation, Shawnee Mission, Kansas 66216, USA; 15 mg/kg п/к 1 раз в день). На следующий день после введения препаратов птица уселась, распределив вес равномерно на обе тазовые конечности, и ела самостоятельно.
В течение последующих 14 дней у птицы развивалась двусторонняя атаксия тазовых конечностей, которые регрессировали до клинических признаков, гиперфлексии и мышечной ригидности, схожими с теми, которые были обнаружены при первичном неврологическом обследовании. Птица не могла встать, однако сохраняла способность балансировать на тибиотарсальном-тарзометаразальных суставах обоих тазовых конечностей в сидячем положении. Мышечный тонус и движение, в том числе защитное оборонительное поведение, рефлексы отдергивания и поверхностная болевая реакция обоих крыльев оставались сохраненными. Поведение, ориентация, аппетит, движения головы и шеи и ментальный статус были адекватными. Многократные повторные ОАК были с минимальными изменениями. Последний ОАК был выполнен на 22 день и показал лишь незначительное снижение лейкоцитоза (28.07×10 3/мкл) и гетерофилии (18.8×10 3/мкл). Развились генерализованные подергивания мышц тазовых конечностей и неспособность балансировать на тибиотарзально-тарзометатарзальном суставе; птица была эвтаназирована на 27 день и было проведено полное патологоанатомическое вскрытие.
На общем осмотре каудальная половина шеи была ригидной, изогнутой и не могла быть исправлена вручную. Позвоночный канал на уровне C8-С9 был латерально компрессирован, уменьшив диаметр спинного мозга примерно на 70% (Рис. 2). Посмертные рентгенограммы позвоночного столба выявили смещение тех же сегментов шейных позвонков, выявленные при общем осмотре, а также потерю нормальной архитектуры и склеротические изменения, невыявленные на первичной рентгенограмме. Выявлено 1,2×1.5 см сросшиеся гранулемы внутри левого подключичного воздушного мешка и в краниальной части левого легкого; образцы из левого легкого были взяты для посева на аэробных/анаэробных средах и определения антибиотикочувствительности; росло подозрение на инфекцию, вызванную Mycobacterium sp.. Собранные рутинные образцы тканей (гол.мозга, глаз, легких, печени, поджелудочной железы, селезенки, почек, сердца, надпочечников, скелетной мышцы, жкт, костного мозга и костей) зафиксированы, заключены в парафин, нарезаны на микротоме (толщиной 5 мм), окрашены гематоксилином и эозином. Пораженные части левого легкого, позвоночного столба и спинного мозга были окрашены по Цилю–Нильсену.

Гистопатологическое исследование шейного отдела позвоночника выявило многоочаговые и сливные гранулемы, заполняющие межбалочные пространства (Рис. 3). Гранулемы имели некротизированное ядро, окруженное гигантскими многоядерными клетками и эпителиоидными макрофагами, которые деформировали и заменили окружающие кости. Вокруг некротизированного ядра смешанная популяция лимфоцитов, плазматических клеток, редкие гетерофилы и тканевые макрофаги, окруженные фиброзной капсулой. В макрофагах обнаружены кислотоустойчивые бациллы (Рис. 3A).

Сливающиеся гранулемы сдавливали спинной мозг на уровне С8–С9, вызвая значительное уменьшение как белого, так и серого вещества (Рис. 3B).

Поражения спинного мозга характеризовались некрозом нейронов с аксональной и миелоидной дегенерацией и макрофагальной инфильтрацией (валерианова дегенерация). Также наблюдалась микроглиальная и астроцитарная пролиферация и активация. Краниальнее от компрессии (на уровне С6) валерианова дегенерация поражала приблизительно 30% дорсального, 60% латерального и 50% вентрального канатиков. Каудальнее компрессии (на уровне С11) валерианова дегенерация затрагивала приблизительно 10% латерального и 50% вентрального канатиков. Очаговое гранулематозное воспаление присутствовало в оболочках, нервных корешках и ганглиях.
Кислотоустойчивые бациллы были выявлены в гранулемах из: краниальной части левого легкого, левого подключичного воздушного мешка, из спинного мозга шейного отдела позвоночника и прилегающего позвоночного столба. Дополнительно был выполнен посев специально на Mycobacterium spp. из левого легкого и левого подключичного воздушного мешка. Легочную ткань обрабатывали по методике, описанной ранее, и впоследствии инокулировали в BACTEC 12B и MGIT 960 (Becton Dickenson, Sparks, Maryland 21152, USA) жидкие среды и на твердые среды Lowenstein–Jensen (Becton Dickenson). Кислотоустойчивые организмы были высеяны из обоих жидких сред после культивирования в течение 10 дней. ДНК, извлеченная из изолятов, была подвергнута частичному rpoB секвенированию. 734-bp фрагмент был сравнен с референтной последовательностью GenBank (NCBI, Bethesda, MD, USA). Генетические дендрограммы были созданы с использованием программного обеспечения MEGAversion 5.0 (онлайн версия доступна тут: www.megasoftware.net) из 1,000 загрузочных репликаций. rpoB фрагмент на 100% соответствовал референсному штамму Mycobacterium avium подвиду avium ATCC 25291. Зафиксированная в парафине спинномозговая ткань была обследована методом ПЦР в реальном времени (real time PCR) и была положительна на M.avium комплекс.
Этот случай представляет собой очень необычное проявление хорошо документированного заболевания. У краснохвостого сарыча в удовлетворительном состоянии были симптомы острой травмы позвоночника, не было синяков/гематом, иногда свидетельствующих о травме позвоночника у птиц. Многочисленные исследования в 27-дневный стационарный период не выявили специфических патологий шейных позвонков; однако глубоко пальпировать каудальную часть шейного отдела позвоночника затруднительно. Лейкограмма показывала умеренный лейкоцитоз (по сравнению со многими случаями микобактериоза птиц), поэтому первичный диагноз был поставлен исходя из предположения о травме, которую получила птица. У птицы не было признаков затрудненного дыхания в течение всего периода госпитализации, и первоначальные рентгенограммы не имели заметных отклонений в респираторной системе или в каудальной части шейного отдела позвоночника.
Классические клинические признаки микобактериоза у диких хищников включают: анорексию, прогрессирующую потерю веса, атрофию мышц, тусклые и взъерошенные перья, слабость, диарею, выпячивание брюшной стенки и вялость – и ничто из этого не было выражено в данном случае. Кроме того, в этом случае не было классических общих или гистопатологических микобактериозных поражений желудочно-кишечного тракта.
Прогрессирующие неврологические клинические признаки были вызваны, скорее всего, разрушением каудальных шейных позвонков, которая привела к компрессии шейного отдела спинного мозга и последующей сегментарной недостаточности. Количество позвонков и, соответственно, число сегментов спинного мозга варьирует у разных видов, таким образом поражения шеи могут или не могут затрагивать шейное утолщение. Многие виды хищных птиц имеют 14 шейных позвонков, но точное число шейных позвонков краснохвостого сарыча в литературе не уточняется. Однако, один из авторов упомянул, что у этих канюков 12 шейных и 8 грудных позвонков, и шейное утолщение находится в промежутке от С10/11–С12/Т1 (Armie´n, личное сообщение.).
У этой птицы ожидались проявления признаков поражения верхних двигательных нейронов тазовых конечностей и крыльев. Признаки повреждения верхнего мотонейрона, выявленные в тазовых конечностях, включали чрезмерные рефлексы, ригидность мышц разгибателей, нормальную интенсивность рефлекса отдергивания, поверхностную болевую реакцию и парез. В сегментах C6-c11 двигательные нейроны были интактные, но проприоцептивные проводящие пути были поражены, как и вестибулоспинальный тракт. В связи с повреждением этих участков можно было бы ожидать проприоцептивный дефицит и дискоординацию движения крыльев; однако неврологические аномалии не были выявлены ни на одном из крыльев в течение многочисленных неврологических осмотров. Птица проявляла защитное поведение и хлопала крыльями при манипуляциях с ней. Возможно, что она имела незначительный дефицит функции верхнего двигательного нейрона, который клинически не проявлялся.
Кислотоустойчивые микроорганизмы были выявлены как в респираторной системе, так и в тканях позвоночного столба; таким образом, имеется два возможных пути заражения. Первый – чрезкожное заражение вследствие тупой травмы или раны кожи с последующим распространением в позвоночник и легкие. Так как позвонки пневматизированы, чрезкожный путь мог позволить возбудителю распространиться от позвонков в респираторную систему или наоборот. Но никаких следов внешних ранений не было обнаружено в данной области. Второй – респираторный путь (путем вдыхания возбудителя). Первичная респираторная инфекция возникла непосредственно в воздушных мешках с последующим гематогенным распространением, однако этот путь менее вероятен из-за отсутствия общих гистологических патологий, связанных с микобактериозом в других тканях.
Обычные клинические признаки микобактериоза хищных птиц при поражении центральной нервной системы редки, но включают в себя: невозможность летать, вялость, прогрессирующие неврологические признаки, слабость мышц, судороги и опистотонус. Насколько известно авторам, существует только одна публикация о случае поражения шейных позвонках у хищной птицы; поражения на уровне C1-2 были связаны с атаксией, гиперрефлексией и чрезмерным разгибанием тазовых конечностей.
Таким образом, несмотря на редкость, микобактериоз следует рассматривать как дифференциальный диагноз при периферическом неврологическом дефиците у диких хищных птиц, будь то острый либо хронический. Кроме того, неврологическая оценка крыльев может быть трудной для интерпретации диких хищных птиц, поэтому незначительные неврологические нарушения могут быть незамеченными.
Благодарности: Авторы благодарят Dr. Suelee Robbe-Austerman и Jim Higgins из the National Veterinary Services Laboratory в Ames, Iowa за из помощь в выделении и секвенировании Mycobacterium avium avium, а также Dr. Allison Zwingenberger и Dr. Dennilyn.
На заглавном фото молодой краснохвостый сарыч (Buteo jamaicensis) By Jason Crotty (Flickr: Red-Tailed Hawk) [CC BY 2.0], via Wikimedia Commons
